| カテゴリー | 医学、基礎 |
|---|---|
| 代表研究者 | 近藤 和也 |
| 関連する研究者 |
滝沢 宏光
吉田 光輝
森田 明典
丹黒 章
副島志帆(大学院博士後期課程2年生)
Bilguun Tegshee(大学院博士後期課程2年生)
六車京香(大学院博士前期課程2年生)
Max Costa (NYU School of Medicine Professor)
Chengfeng Yang (University of Kentucky Professor)
John Pierce Wise (University of Louisville Professor)
|
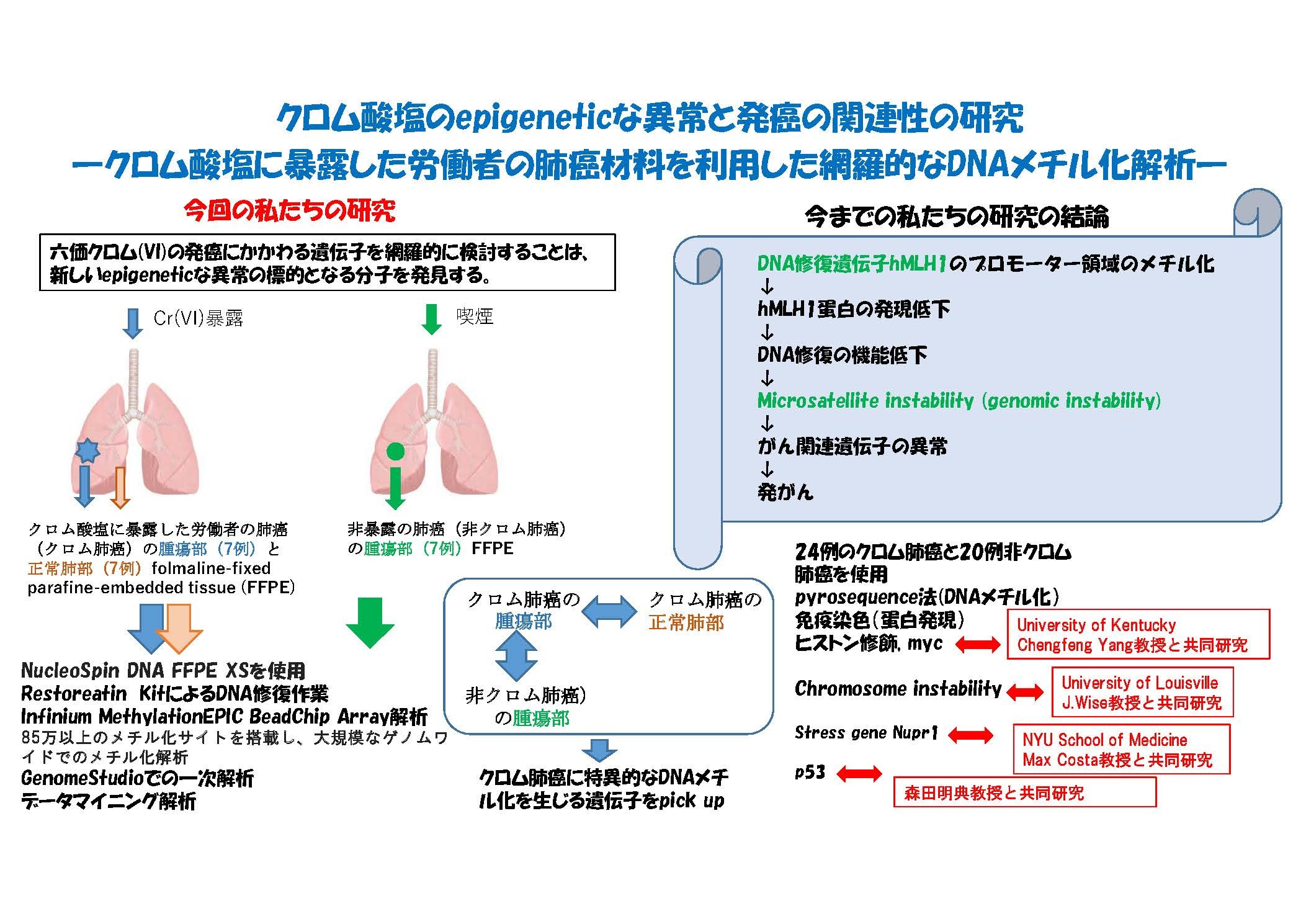
| 研究概要 | Cr(VI)(六価クロム)は、最もよく知られた環境汚染の発癌物質の一つで、International Agency for Research on Cancer (IARC)はCr(VI)をgroup Iのヒト発癌物質に認定している(1)。肺癌や他の癌の原因となることはよく知られているが、その発癌のメカニズムは、明らかでない(2)。Crの職業性暴露は、米国では約50万人が、全世界では数100万人あると報告されている(1)。ジュリア・ロバーツが主演した映画『エリン・ブロコビッチ』 (2000年)では、六価クロム溶液の土壌汚染が問題となっている。アメリカで、工場の敷地内に高濃度の六価クロム溶液を10年以上大量に垂れ流していた企業があって、地域の地下水を汚染し、周辺住民に癌などの健康被害が多発した。さらに、Crによる海洋汚染が進行している。エジプトの3つの都市はCrの高いレベルを報告している(Tabbin; 5.266µg m-3, Ramsis; 4.231µg m-3, Shoubra; 6.842 µg m-3) (3)。共同研究者のWise教授は、全世界の海洋に住むクジラの精子を集め、Cr濃度を測定した。太平洋のthe Islands of Kiribati (mean = 44.3 ± 14.4 µg/g)やインド洋のSeychelles (mean = 19.5 ± 5.4 µg/g)では、最も高いレベルのCrを観察した。クジラの精子のCr濃度は、肺癌で死亡するクロム労働者の正常肺組織と同じレベルであることを報告している(4)。Crによる汚染が土壌だけでなく、海洋にも進行していることを警告している。 たくさんのin vitroや動物実験からCr(VI)は容易に細胞内に入り、その代謝還元物やreactive oxygen speciesがgeneticな異常を促進することが知られ、発癌の一つの原因と考えられている(5)。最近、Cr(VI)の暴露で様々なepigeneticな異常を生じることが報告されている(6, 7, 8, 9)。epigeneticな異常は、DNA methylation、histone modificationやnon-coding RNAによる標的遺伝子の発現の変化である。 Kleinらは、2002年に最初にCr(VI)暴露によりDNAメチル化が高くなり、標的遺伝子の発現が抑えられることをin vitroで証明した(10)。Labraらもこの現象を指示した(11)。さらに、Cr(VI)の暴露がhistone modification の原因となることが示された(12, 13, 14)。これらの研究はin vitroで行われた。 私たちは、クロム酸塩に暴露した労働者の肺癌(クロム肺癌)35例と非暴露の肺癌(非クロム肺癌)26例の材料を使用し、癌抑制遺伝子hMLH1とp16のDNAメチル化を検討し、クロム肺癌で有意に高いことを報告した(15, 16)。hMLH1遺伝子のDNAメチル化がその蛋白発現を低下させ、修復遺伝子としての機能を阻害し、microsatellite instability (MSI)を促進し、癌関連遺伝子の異常を高め、発癌となることを報告した(17, 18)。さらに、クロムに暴露した正常肺のhMLH1遺伝子のDNAメチル化が対象群より高値であった(19)。私たちの今までの研究で、クロムの暴露が癌抑制遺伝子のDNAメチル化を高め、その遺伝子の発現を低下さすことで発癌を促す、という過程が示唆された。 また、世界中のクロム酸の研究者のほとんどがin vitroまたは動物実験を行い、様々な結果を報告している。しかし、実際、現実にそうなっているかどうか、は不明である。私たちヒトクロム肺癌の材料を持っているので、今まで共同研究してきた。University of LouisvilleのWise教授とは、15年前よりクロム酸のchromosome instabilityについて、University of KentuckyのYang教授とは、15年前よりクロム酸のmyc及びヒストン修飾について、最近、NYU School of MedicineのCosta教授とは、ストレス蛋白Nupr1について共同研究を始めている。 今回はepigenetic な変化の中のDNAメチル化の異常とクロム発癌について網羅的に検索する。この結果と今までのin vitroや動物実験の結果から、現実にクロム発癌にかかわっている遺伝子を同定することができる。 ※参考文献は、以下(徳島大学研究クラスターNo.2004004)にてご覧ください。
▼徳島大学研究クラスターNo.2004004
|
| 研究者の役割分担 | 近藤和也 研究の総括、GenomeStudioでの一次解析、データマイニング解析, 遺伝子のpick up 丹黒 章 研究の助言 吉田光輝 FFPE材料からのDNAの抽出と精製、pyrosequence法によるDNAメチル化測定 副島志帆 FFPE材料からのDNAの抽出と精製、pyrosequence法によるDNAメチル化測定 滝沢宏光 Infinium MethylationEPIC BeadChip array解析 六車京香 Infinium MethylationEPIC BeadChip array解析 Bilguun Tegshee Infinium MethylationEPIC BeadChip array解析 Max Costa クロム肺癌におけるストレス蛋白Nupr1の研究 Chengfeng Yang クロム肺癌におけるmycがん遺伝子の役割, クロム肺癌におけるヒストン修飾についての研究 John Pierce Wise クロム肺癌におけるchromosome instability 森田明典 クロム肺癌におけるP53 |
| 研究期間 | 2020年4月1日〜2023年3月31日 |